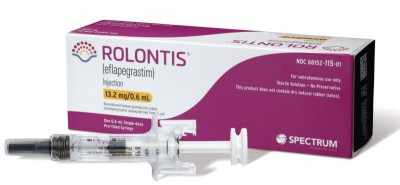
미국 FDA가 한미약품이 스펙트럼에 라이선스 아웃한 바이오신약 '롤론티스'에 대한 허가일정을 잠정 연기했다.
코로나19로 인해 미국 공무원 해외출장 제한 규정이 생기면서 한국 실사(평택 바이오플랜트 대상)를 하지 못해, 지난 24일로 예정됐던 롤론티스 허가일을 지킬 수 없게 됐다.
스펙트럼은 지난 26일(현지시각) "FDA로부터 ‘한국 실사 완료 때까지 롤론티스 허가를 잠정 연기한다’는 통보를 받았다"며 "실사를 신속히 진행할 수 있는 방법을 FDA와 함께 적극적으로 찾고 있다"고 전했다.
평택 바이오플랜트 실사 외에 미국 내 롤론티스 완제 생산처, 완제 포장 사이트, 스펙트럼 본사 대상 FDA 실사는 현재 모두 성공적으로 끝난 상황이며, 요청받은 허가 진행 관련 자료들 역시 제출을 완료해 모든 절차가 마무리된 상태이다.
한미약품은 "FDA가 스펙트럼에 CRL(Complete Response Letter, 중대 결격사유가 있어 허가할 수 없음)이나 '허가 거절(Rejection)'이 아니라 '연기(Defer Action)'라고 통보한 것은 평택 플랜트 실사 외에 허가에 필요한 다른 모든 절차가 성공적으로 마무리됐음을 의미한다"며 "한국 실사 일정이 다시 잡히는대로 FDA 허가 프로세스가 빠르게 가동될 것"이라고 설명했다. 이어 "국내 허가의 경우 이르면 연내에 가능할 것으로 예상한다"고 덧붙였다.
롤론티스는 한미약품이 개발한 호중구감소증치료제로, 미국 제약기업인 스펙트럼에 2012년 라이선스 아웃됐으며, 스펙트럼은 글로벌 임상 3상을 끝내고 작년 10월 FDA에 시판허가를 신청했다.
서희원 기자 shw@nextdaily.co.kr